في هذا الدليل الشامل، سنستكشف معاً مختلف أنواع المواد، من المواد الصلبة والسوائل إلى الغازات والبلازما، وسنغوص في خصائص كل حالة وكيف تؤثر على حياتنا اليومية. سنعتمد على أمثلة واقعية ونظريات علمية، لنقدم لك رؤية متكاملة تسهل عليك فهم هذا المفهوم الأساسي.
وسواء كنت طالباً تبحث عن معلومات دقيقة، أو مهتماً بعلم المادة، فإن هذا الدليل هو نقطة انطلاقك لفهم أعماق المادة وكيف تشكل عالمنا. دعنا نبدأ هذه الرحلة المعرفية سوياً.
تعريف المادة
المادة هي كل ما يتكون من جزيئات وتُستخدم في تشكيل مواد أخرى، وتتميز بخصائص كيميائية وبيولوجية وفيزيائية محددة. يمكن أن تكون هذه المواد في حالات مختلفة؛ غازية، أو سائلة، أو صلبة. كما أنَّها قد تلعب أدواراً متعددة، حيث نجد بعض المواد مفيدة مثل المواد الغذائية، بينما قد تكون أخرى ضارة كالسُّموم. علاوةً على ذلك، توجد مواد يمكن رؤيتها بالعين المجردة، في حين أن هناك مواد أخرى تبقى غير مرئية إلا عند تفاعلها مع مواد أخرى. تتنوع صفات المواد بشكل واسع، مما يجعلها موضوعاً غنياً للدراسة والاستكشاف في مجالات متعددة.
أنواع المادة
يوجد أنواع عديدة للمادة وهي:
1. العناصر
تعدّ العناصر الكيميائية الأساس الذي يقوم عليه تكوين المواد، حيث تتكون كل عنصر من نوع واحد فقط من الذرات. ويبلغ عدد العناصر المكتشفة حتى الآن 118 عنصراً، والتي تُستخدم لتشكيل مجموعة هائلة من المركبات المعقدة التي لا تزال قيد الاكتشاف. بينما تتواجد معظم العناصر في الطبيعة بشكل حر، فإنَّ حوالي 20% منها تُحضّر في المختبرات الكيميائية، وغالباً ما تكون ضئيلة الكمية عند وجودها طبيعياً. ومن الملاحظ أن معظم هذه العناصر صلبة، مثل الحديد والألومنيوم.
تُحدد ذرات العناصر بواسطة عدد البروتونات التي تحتويها، مما يمنح كل عنصر عدداً ذرياً فريداً لا يمكن أن يتشارك فيه عنصران مختلفان. يمكن للمرء أن يتبع هذا التوزيع من خلال الجدول الدوري للعناصر. وتتركب ذرات العنصر أيضاً من الإلكترونات والنيوترونات، حيث تلعب النيوترونات دوراً في وجود نظائر مختلفة للعنصر عند اختلاف قيمتها. وعندما يكتسب العنصر أو يفقد إلكترونات، تتشكل أيونات خاصة به.
للتسهيل في التعامل مع العناصر، يُستخدم رموز لاتينية مختصرة، تتكون عادةً من حرف أو حرفين، بحيث يكون الحرف الأول دائماً كبيراً والثاني صغيراً إن وُجد. على سبيل المثال، يُرمز لعنصر الهيدروجين بـ "H" وللهليوم بـ "He"، مما يسهل التعرف على العناصر في مختلف السياقات الكيميائية.
2. المركبات
تُنتَج المركبات نتيجة تفاعل كيميائي بين نوعين أو أكثر من ذرات العناصر المختلفة، ولا يمكن إعادة تلك المركبات إلى مكوناتها الأساسية بسهولة إلا من خلال تحليل كيميائي يتضمن تفاعلات إضافية. تتحد العناصر لتكوين المركبات عبر إنشاء روابط كيميائية، تتشكل من خلال فقد أو كسب إلكترونات التكافؤ الموجودة في المدار الخارجي لكل ذرة. ترتبط ذرات العناصر في المركب بنسب ثابتة ودقيقة، وتتنوع الروابط الكيميائية التي تجمعها، مثل الرابطة الأيونية، والرابطة التساهمية، والروابط المعدنية، والرابطة التساهمية التناسقية.
يمكن التعبير عن المركب كيميائياً بعدة طرق، إما من خلال الصيغة الجزيئية التي توضح أنواع الذرات وعددها، أو من خلال الصيغة البنائية التي تبرز أنواع الروابط الكيميائية المكونة للمركب. يُعتبر الماء من أشهر المركبات وأكثرها أهمية، حيث يتكون من ذرتين من الهيدروجين وذرة واحدة من الأكسجين بنسبة 2:1، ويتحدد تركيب الماء بواسطة الرابطة التساهمية، ويُعبر عنه بالرمز H₂O. كما تُعد المركبات العضوية مثالاً شائعاً، حيث تتكون أساساً من عناصر الكربون والهيدروجين والأكسجين، مما يعكس تنوع وتعدد أشكال المركبات الكيميائية في الطبيعة.
.jpg_846c61146899fa1_large.jpg)
3. المخاليط
تتكون المخاليط عندما يتم مزج مادتين أو أكثر معاً بطرق ميكانيكية، سواءً كانت عناصر أو مركبات كيميائية، دون أن يحدث تفاعل كيميائي. ومن المهم أن تحتفظ المكونات بخصائصها الأصلية بالكامل. تتميز المخاليط بسهولة إعادة مكوناتها الأصلية، حيث يمكن الفصل بينها باستخدام عمليات فيزيائية تعتمد على الخصائص الفردية لكل مكون، مثل الغليان أو التصفية.
يمكن تقسيم المخاليط إلى نوعين رئيسيين المخلوط المتجانس، الذي تكون فيه جميع خصائصه متساوية في جميع أجزائه، مثل المحاليل التي تتكون من جزيئات صغيرة ذائبة تماماً، كما هو الحال في خليط الماء والسكر أو الماء والملح. أما المخلوط غير المتجانس، فيتميز بعدم توزيع مكوناته بشكل موحد، حيث تختلف خصائصه حسب تركيز المواد، كما نرى في السوائل التي تحتوي على مواد راسبة مثل الماء والحجارة.
من الأمثلة الشائعة على المخاليط هو النفط، الذي يتكون من عدة مركبات عضوية؛ وماء البحر، الذي يحتوي على أنواع متعددة من الملح والماء؛ والهواء، الذي يتكون من مجموعة من الغازات مثل الأكسجين والنيتروجين وثاني أكسيد الكربون؛ والحبر، الذي يتألف من مزيج من الصبغات المختلفة. كما أنّ البارود يتكون من الكبريت ونترات البوتاسيوم والكربون. تعكس هذه الأمثلة تنوع المخاليط وكيفية تأثير مكوناتها المختلفة على خصائصها العامة.
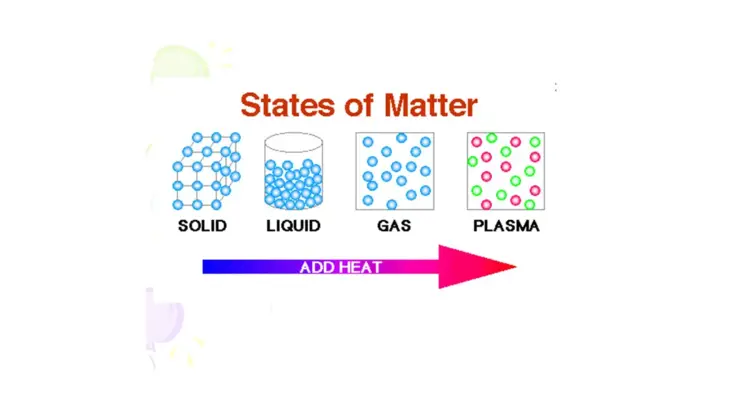
حالات المادة
يوجد للمادة اربع حالات وهي:
1. المادة الصلبة
تتميز الحالة الصلبة للمادة بخصائص فريدة تجعلها ذات شكل وحجم محددين، ويرجع ذلك إلى الترابط القوي والوثيق بين الجزيئات المكونة لها. هذه الجزيئات، التي تتحرك ببطء، تمنح المواد الصلبة استقراراً واضحاً، وغالباً ما تتخذ هذه المواد أشكالاً بلورية. من بين الأمثلة الشائعة على المواد الصلبة البلورية نجد السكر وملح الطعام والألماس، بالإضافة إلى مجموعة متنوعة من المعادن.
كذلك تشمل الحالة الصلبة مواد أخرى مثل الصخور والأخشاب عند درجة حرارة الغرفة. تتشكل المواد الصلبة عادةً عند تبريد المواد السائلة أو الغازية، كما يتضح من تحول الجليد، الذي يمثل مثالاً واضحاً على انتقال المادة من الحالة السائلة إلى الحالة الصلبة بفعل انخفاض الحرارة.
.jpg_e5347c0f16462bd_large.jpg)
2. المادة السائلة
تتميز المواد في الحالة السائلة بحجم محدد، لكنها تأخذ شكل الوعاء الذي تحتويها، مما يعني أن شكلها ليس ثابتاً. من أبرز الأمثلة على المواد السائلة الماء والنفط. يمكن أن تتشكل المواد السائلة من خلال تبريد الغازات، كما يحدث مع بخار الماء، حيث يتباطأ حركة جزيئات الغاز بفعل البرودة، مما يؤدي لفقدان الطاقة وتحولها إلى حالة سائلة.
كذلك، يمكن أن تتحول المادة من الحالة الصلبة إلى السائلة عند تسخينها، كما هو الحال مع الحمم المنصهرة، التي كانت في الأصل صخوراً صلبة وتحولت إلى سائل نتيجة التعرض لدرجات حرارة مرتفعة. هذه التحولات تجعل من الحالة السائلة موضوعاً مثيراً يستحق المزيد من الاستكشاف.
3. المادة الغازية
تتميز الحالة الغازية بوجود مسافات واسعة بين جزيئات المادة، مما يمنحها كمية كبيرة من الطاقة الحركية. عندما تكون هذه الجزيئات حرة، تنتشر بشكل غير محدود، في حين أنّها تتوسع لملء الوعاء الذي تحتويه عند وجودها في مكان مغلق. يمكن ضغط الغاز عن طريق تقليل حجم الوعاء، مما يقلل المسافة بين الجزيئات ويزيد من الضغط الناتج عن تصادمها.
كما يمكن زيادة الضغط من خلال رفع درجة الحرارة مع الحفاظ على حجم الوعاء ثابتاً. تتمتع جزيئات الغاز بطاقة حركية كافية تمكنها من التغلب على قوى الترابط التي تربط الجزيئات في المواد الصلبة والسوائل، مما يؤدي إلى عدم امتلاك الغاز لشكل أو حجم محدد.
4. البلازما
في الآونة الأخيرة، بدأ العلماء في استكشاف حالة المادة تحت ظروف درجات حرارة وضغط مرتفعين للغاية، والتي تتواجد عادةً على سطح الشمس أو في الفضاء. في هذه الظروف القاسية، تتفكك الذرات وتفقد إلكتروناتها، مما يؤدي إلى تكوين أيونات ذات شحنة موجبة. يُعرف الخليط الناتج من الذرات المتعادلة، والأيونات المشحونة، والإلكترونات الحرة بالبلازما، وهي الحالة الرابعة من المادة.
تتميز البلازما بخصائص فريدة تجعلها تتصرف كالسائل أو الغاز، كما أنّها تستجيب للقوى الكهربائية والمغناطيسية بسبب وجود الجسيمات المشحونة فيها. تتضمن معادلات ميكانيكا السوائل، المعروفة بمعادلات بولتزمان، كلاً من القوى الكهربائية والمغناطيسية، بالإضافة إلى قوى السوائل التقليدية الموجودة في معادلات نافييه-ستوكس، مما يبرز تعقيد وسحر هذه الحالة الفريدة من المادة.
مكونات المادة
المكونان الرئيسيان للمادة هما:
1. الذرات
تتألف جميع المواد من وحدات أساسية تُعرف بالذرات، التي تتجمع معاً لتشكل العناصر، وذلك بتكوين نوع واحد من الذرات. تتفاعل هذه العناصر، بدورها، لتكون الجزيئات والمركبات المختلفة. تُعدّ الذرة أصغر جسيم في العنصر، وتحافظ على جميع الخصائص الكيميائية والفيزيائية الخاصة به.
تتكون الذرة من نواة موجبة الشحنة، تضم البروتونات والنيوترونات، محاطة بسحابة من الإلكترونات سالبة الشحنة. ورغم أن نواة الذرة صغيرة وكثيفة مقارنة بالإلكترونات، فإن هذه الأخيرة تُعد أخف الجسيمات المشحونة في الطبيعة، حيث ترتبط بالنواة من خلال قوى كهربائية تجذبها، مما يضمن تماسك البناء الذري.
2. الجزيئات
تتجمع الذرات معًا في مجموعات لتشكيل الجزيئات، وعندما تتضمن الجزيئات ذرات من أنواع مختلفة، تُسمى بالمركبات. على سبيل المثال، يتكون مركب الماء من ارتباط ذرتين من الهيدروجين مع ذرة واحدة من الأكسجين، مما يبرز كيفية تفاعل العناصر المختلفة لتكوين مواد جديدة.
هناك نوعان أساسيان من الروابط التي تربط بين الذرات لتشكيل هذه الجزيئات: الروابط الأيونية، التي تتضمن تبادل الإلكترونات، والروابط التساهمية، حيث تشترك الذرات في الإلكترونات. هذه الروابط تؤدي دوراً حيوياً في تحديد خصائص المركبات وسلوكها الكيميائي.
الجدول الدوري للعناصر
يُعدّ الجدول الدوري ترتيباً للعناصر الكيميائية بناءً على العدد الذري (عدد البروتونات في النواة). يوضح الجدول الخصائص الدورية للعناصر، حيث تتشابه عناصر المجموعة نفسها في السلوك الكيميائي.
- المجموعات: الأعمدة الرأسية في الجدول الدوري. وتحتوي على عناصر لها خصائص كيميائية متشابهة.
- الدورات: الصفوف الأفقية. وتمثل تدرجاً في الخصائص الكيميائية والفيزيائية.
- الكواركات: مكونات البروتونات والنيوترونات. تأتي في ست أنواع هي علوي، وسفلي، وغريب، وساحر، وقاعي، وقمي.
- البوزونات: جسيمات تحمل القوى الأساسية في الطبيعة، مثل الفوتون (يحمل القوة الكهرومغناطيسية).
- النيوترينوات: جسيمات خفيفة جداً، تتفاعل بشكل ضعيف مع المادة.
الجسيمات دون الذرية
هذه المكونات والجسيمات تؤدي دوراً أساسياً في تكوين وفهم المادة والطاقة في الكون.
خصائص المادة
للمادة خصائص مختلفة:
1. الخصائص الفيزيائية
تعتبر الخواص الفيزيائية من السمات الأساسية التي تصف كيفية تطور وتحول نظام فيزيائي في لحظة معينة، مما يمكننا من قياسها وملاحظتها دون التأثير على مكونات المادة نفسها. تنقسم هذه الخواص إلى نوعين رئيسيين هما الخواص الفيزيائية المكثفة، التي تظل ثابتة بغض النظر عن كمية المادة أو حجمها، مثل الكثافة التي تقاس بوحدات الكيلوغرام لكل متر مكعب، والحرارة النوعية التي تقاس بالجول لكل مول.
من جهة أخرى، توجد الخواص الفيزيائية الشمولية، التي تعتمد على حجم أو كمية المادة، حيث تزداد قيمتها مع زيادة حجم المادة أو كميتها، مثل المحتوى الحراري وعدد الجسيمات. هذا التمييز بين الأنواع المختلفة للخواص الفيزيائية يساعدنا في فهم سلوك المواد وتفاعلها في مختلف الظروف.
2. الخصائص الكيميائية
تُعرف الخاصية الكيميائية بأنّها سمة غير مرئية للمادة يمكن تمييزها من خلال الحواس، حيث تؤدي دوراً حيوياً في تحديد سلوك المادة أثناء التفاعلات الكيميائية. تعكس هذه الخاصية قدرة المادة على التفاعل مع مواد أخرى أو التحول إلى مادة جديدة تماماً. وبالتالي، تمثل الخاصية الكيميائية جوهر التفاعلات التي تحدد كيفية تغير المواد وتفاعلها في مختلف الظروف، مما يجعل فهمها أمراً أساسياً لكل من يهتم بعالم الكيمياء.
3. الخصائص النووية
تُعدّ الخواص النووية للمادة من الأمور الحيوية التي تلعب دوراً رئيسياً في فهم التفاعلات النووية واستخداماتها المتنوعة. تشمل هذه الخواص القدرة على التفاعل النووي، إذ تتمتع المادة النووية بإمكانية إصدار إشعاعات نووية نتيجة لتفاعلاتها. كما أن بعض النظائر النووية تتمتع باستقرار نسبي، مما يعني أنّها لا تتحلل تلقائياً، بينما توجد نظائر أخرى غير مستقرة تتحلل من خلال الإشعاعات النووية.
كما تتميز المادة النووية أيضاً بإطلاق كميات هائلة من الطاقة أثناء التفاعلات النووية، مما يجعلها مصدراً قوياً للطاقة. علاوةً على ذلك، يمكن تحويل النظائر النووية من نوعٍ إلى آخر عبر الإشعاع النووي، مما يتيح إمكانيات واسعة في التطبيقات المختلفة.
في الختام
في ختام هذا الدليل الشامل حول تعريف المادة وأنواعها وحالاتها وخصائصها، نكون قد غطّينا الأسس الأساسية لفهم هذه الظاهرة المعقدة والمذهلة. فالمادة ليست مجرد شيء نتفاعل معه يومياً؛ بل هي جوهر الكون من حولنا.
ندعوك لمواصلة رحلتك في عالم العلوم، فكل اكتشاف جديد يمنحنا رؤى أعمق حول المادة ودورها الحيوي في حياتنا اليومية. نأمل أن يكون هذا المقال قد أضاف إلى معرفتك وألهمك لاستكشاف المزيد في عالم الكيمياء والفيزياء.




أضف تعليقاً